Изобретение первых аккумуляторов
Аккумулятор – это прибор для накопления энергии с использованием химических реагентов, которую впоследствии можно переводить в форму электрической. Система работы аккумулятора основывается на использовании двух видов металла и кислотного раствора. Взаимодействие их между собой в такой среде, собственно, и вырабатывает электричество.
Происхождение слова «аккумулятор», как и большинства других технических понятий, берет начало из латинского языка. В переводе оно значит «собиратель». Этим термином называют такие устройства, чьё главное назначение – накопление энергии и дальнейшее её использование. Аккумуляторы не ограничиваются лишь электрическими приборами. К примеру, обычная растянутая или сжатая пружина является самым простым аккумулятором, накапливая внутри себя механическую энергию. Другим типом такого устройства есть раскрученный маховик, который таким способом хранит в себе энергию кинетическую.
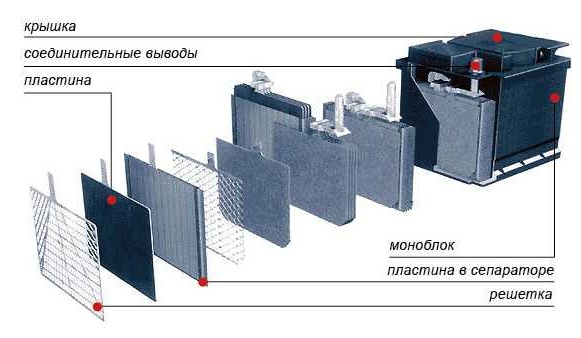
Краткое описание устройства автомобильного аккумулятора
Устройство автомобильного аккумулятора из чего состоит авто аккумулятор
1 – корпус-моноблок, который изготавливают из эбонита или другого материала устойчивого к кислоте
2 – верхняя крышка аккумуляторной батареи
3 – положительный выход (клемма) которая имеет больший диаметр, чем отрицательный (5) – это необходимо для исключения перепутать плюсовой и минусовые клеммы, чтобы не допустить замыкание
4 – межэлементные короткие соединения, необходимы они для соединения пластин (9)
5 – отрицательная клемма меньше по диаметру, чем положительная
6 — пробки, обычно полиэтиленовые с небольшим отверстием для вентиляции
7 – электролит должен всегда быть заполненным до определённого уровня обычно указывается на батареи полоской
8 – разделительные сепараторы, которые вставляются между положит. И отриц. пластинами
9 – положительные и отрицательные пластины, которые чередуются, а между ними вставляются сепараторы
10 – Борн — он соединяет малые аккумуляторные блоки в единую батарею (их два – один соединяет положительные, другой отрицательные) которые в свою очередь выводятся в клеммы
Устройство аккумуляторной батареи ноутбука
Аккумулятор для ноутбука состоит внутри из нескольких батарей, соединённых между собой, в основном эти батареи Li-ion – ного типа. Из электрической схемы, её задача осуществлять контроль за уровнем зарядки или разрядки аккумуляторных элементов. Контроллер — определяет ёмкость батареи, считает количество циклов заряжения и разряжения аккумулятора для ноутбука и измеряет температуру литий-ионных батарей.

Аккумулятор для ноутбука — устройство
Виды батареек:
1 — сухие — это угольно цинковые или солевые батарейки, которые производятся массово и стоят дешевле остальных
2 — щелочные это щелочно-марганцевые и алкалиновые батарейки, они средние по цене и производству, но по качеству немного превосходят первый вид (сухие)
3 — литиевые — самые дорогие по цене, но преимущество очевидно: такие батарейки хорошо работают как при низких, так и при высоких температурах, они лёгкие по весу и более долговечные, чем предыдущие два вида.
Батарейки бывают различных размеров типов и отличаться энергоёмкостью — более подробно эти характеристики будут описаны в ближайших статьях.
А также мы расскажем обо всех аккумуляторных батареях, о том как правильно, где их лучше приобрести, о зарядке батарей и рассмотрим другие вопросы, связанные с аккумуляторами и зарядными устройствами для них.
Основные характеристики аккумуляторов
основными характеристиками являются: электрическая ёмкость, напряжение, внутреннее сопротивление, ток саморазряда и, естественно, срок использования. Есть и другие характеристики, их мы подробнее рассмотрим в других статьях нашего сайта.

Аккумуляторная ёмкость
Первый и самый важный показатель аккумулятора – это его ёмкость, то есть то количество энергии, которое он имеет при полной зарядке. Понятно, что чем выше этот параметр у данного устройства, тем дольше можно использовать приборы, которые на нем работают, без дополнительной подзарядки. Единица измерения ёмкости – один миллиампер-час (мА.час). На каждом аккумуляторе или на его упаковке всегда указывается его номинальная ёмкость
Но фактически реальное количество электрической энергии в аккумуляторе всегда меньше заявленного номинального показателя. Реально же ёмкость устройства составляет от 80% до 110% этого значения. Чем дольше используется аккумулятор, тем сильнее меняется данная характеристика – то есть, ёмкость его потихоньку уменьшается. Частые причины такого уменьшения – нарушение технологии первого использования, нарушения в процессе эксплуатации, качество зарядных устройств и продолжительность эксплуатации, и многое другое.
Внутреннее сопротивление аккумуляторов
Это второй по значению показатель качества аккумулятора. Единица измерения внутреннего сопротивления – миллиомы (мОм). В зависимости от разных факторов – ёмкости устройства, разных используемых металлов, количества элементов, правильной или неправильной эксплуатации аккумулятора – эта величина может меняться. Измеряют её с помощью специальных приборов, которые изготавливают разные производители, такие, к примеру, как Cadex.
С увеличением времени использования аккумулятора величина внутреннего сопротивления меняется в сторону увеличения. К примеру, если сопротивление аккумулятора равно 500 мОм, то это значит, что устройство сильно устарело или длительное время эксплуатировалось с нарушениями. Чем выше показатель внутреннего сопротивления, тем меньше времени он будет полноценно функционировать.
Если вспомнить о законе Ома, то становится понятно, что чем больше внутреннее сопротивление аккумулятора, тем сильнее падает напряжение на приборе, который работает на нем. Когда напряжение достигает определённого уровня, этот прибор будет считать, что аккумулятор разрядился полностью, и отключится.
Вот почему при повышении внутреннего сопротивления аккумулятор выдаёт все меньше своей накопленной энергии, вследствие чего прибор начинает работать меньше времени.

Саморазряд аккумулятора
Следующий показатель – это то количество внутренней энергии аккумулятора, которое он со временем теряет самопроизвольно после полноценной зарядки. Такая потеря – естественное явление для абсолютно всех видов аккумуляторов, она не зависит от типа электрохимических систем. Чтобы как-то оценить размеры саморазрядки количественно, величину этой утерянной энергии относят к значению показателя непосредственно после зарядки и выражают в процентах.
Первые сутки после полной зарядки размер саморазряда достигает максимального значения. Со временем он очень сильно уменьшается. Поэтому саморазряд и оценивают за 24 часа и за месяц. Кроме того, стоит отметить, что на показатель саморазряда влияет температура окружающей среды – при её увеличении он также растёт.
Если температура воздуха поднимется на 10 градусов, то показатель саморазряда вырастет почти вдвое. Для качественных Ni-Cd приборов допускается саморазряд аккумулятора до 10% на протяжении первых 24 часов, для аккумуляторов Ni-MH типа – чуть больше, а вот для Li-ion и Li-Pol саморазряд почти незаметный, и оценить его можно лишь через месяц. За 30 дней службы аккумуляторы типа Ni-Cd могут иметь до 20% саморазряда, у Ni-MH аккумуляторов этот показатель составляет до 30 %, а литиевые приборы теряют не больше 10 % накопленной энергии.
Срок использования аккумуляторов
Срок эксплуатации аккумуляторов измеряют, как правило, тем, сколько циклов заряда и разряда он может выдержать без критического снижения своих главных характеристик – ёмкости, внутреннего сопротивления и саморазряда. Кроме того, время службы устройства также определяют в зависимости от даты его изготовления. Особенно важно это для литий-ионных (Li-ion) аккумуляторов.
Уменьшение ёмкости аккумулятора до 60% – 80% от заявленного номинального значения свидетельствует о том, что устройство отработало свой срок. Время эксплуатации аккумулятора зависит от многих показателей. Это и тип электрохимической системы, способ заряда, насколько глубоко он разряжался, в каких условиях использовался и других факторов.
Изобретение первых аккумуляторов
Чтобы проследить за историей появления первых аккумуляторов, придётся возвратиться в далёкие времена, когда была создана первая батарея. Александр Вольта в начале 19 века сделал первый и значительный шаг к созданию аккумулятора. Он создал первую батарею, которая привлекала большое внимание физиков тех времён, увлекающихся электрическими опытами. Открытие Вольтой стало сенсацией во всё научном мире того времени. Изобретённый им химический источник постоянного тока получил название «Вольтов столб». Благодаря этому открытию, электрохимическая наука набрала высокие темпы и открытия в этой области стали следовать один за другим.
Очень скоро, спустя год или два, Готеро, учитель музыки, живший в Париже, экспериментируя с разложением воды на кислород и водород, используя вольтов столб, обнаружил, что две проволочки из золота соединённые вместе, после его экспериментов при прикладыванию к языку имеют тот же эффект, что и батарея Вольты, но немного слабее.
По прошествии нескольких лет к этому опыту вернулся Иоганн Вильгельм Риттер, немецкий фармацевт. Однако он пошёл дальше, соорудив из сорока медных кружков столбик, подлаживая под каждый кружок суконку, смоченную подкислённой водой. Соединив полюса получившегося столбика с вольтовой батареей, он получил потрясающий эффект: вся, сделанная им конструкция зарядилась электричеством.
Это открытие привлекло к себе многих и в 1839 году английский физик Грове изобрёл газовый вторичный элемент, который после зарядки от постоянного источника давал ток. Батарея состояла из платиновых электродов, на одном из которых при заряде скапливался водород, а на другом кислород. Электролитом в этом элементе служила серная кислота. При разрядке батареи происходила обратная реакция: водород окислялся, а кислород восстанавливался. Напряжение батареи было около 1В. Изобретение Грове стало прототипом топливных элементов, но широкого распространения оно не получило.
Элемент газовый Грове
В 1859-1860 годах в лаборатории Александра Беккереля, который являлся французским физиком, работал никем не известный в те времена ассистент знаменитого физика — Гастон Плантэ. Молодой человек интересовался улучшением вторичных элементов, которые могли бы стать надёжными источниками в области телеграфии. Он изменил батарею Грове, заменив платиновые элементы на свинцовые, а позже после экспериментов оставил лишь две тонкие свинцовые пластины, которые переложил суконным материалом и намотал на деревянную палочку, вставив это всё в стеклянную банку с электролитом. После подключения пластин к батарее, он заметил, что вторичный элемент не только зарядился, но и сам способен давать ток постоянной силы. Заряд электричества мог на нём сохранятся длительное время при условии, если его сразу не разряжали. Это была первая перезаряжаемая кислотно-свинцовая батарея. Именно эти накопители энергии стали первыми аккумуляторами. Они могли запасать незначительное количество электричества. Однако в ходе экспериментов Плантэ обратил внимание, что если заряженный прибор разрядить, а потом пропустить электрический ток в обратном направлении, повторяя это действие не один раз, то ёмкость аккумулятора при этом значительно увеличивается. Этот процесс получил название — формовка пластин. Чем большая поверхность пластин соприкасалась с электролитом, тем сильнее оказывался ток прибора.
Первые аккумуляторные батареи
Камилл Фор не имел специального образования, но главным его увлечением уже с юных лет была техника. Он работал у Плантэ, наблюдал за его опытами и хорошо уяснил, что ток аккумулятора зависит от величины площади электродов. Чем больше площадь, тем больше ток.
В 1878 году, посетив в Париже выставку, у Фора появилась идея создания нового способа формовки пластин. Он стал покрывать пластины свинцовым суриком, оксидом свинца. В результате этого, при зарядке, сурик, находящийся на одной пластине превращался в перекись, а на другой раскалялся. Окисел на пластине имел пористое строение, которое увеличивало площадь взаимодействия с кислотой. В результате этого эксперимента процесс формовки стал происходить значительно быстрее. По сравнению с аккумуляторами Плантэ, аккумуляторы, изобретённые Фором, имея тот же вес, запасали намного порядков больше электрической энергии.
Именно Фор сконструировал первый электромобиль, имеющий аккумуляторную батарею и развивающий скорость 100км/час. Именно он стал производить первые автомобильные аккумуляторы, которые пользовались широким спросом.
Суть процесса аккумулирования энергии с применением свинцово-кислотной батареи почти не изменилась. Поменялись лишь материалы, которые в настоящее время используют при её производстве.
Кроме свинцово-кислотных аккумуляторов, благодаря экспериментам Томаса Алвы Эдисона, появился железоникелевый аккумулятор, в котором отрицательный электрод сделан из пористого железа или кадмия и который имеет большую рабочую поверхность. Положительный электрод сделан из никеля и окружён окисью трёхвалентного никеля. КПД у такого аккумулятора меньше, чем у свинцового, стоимость его дороже, но он лучше переносит перегрузки, прочен и не нуждается в ремонте.
Однако наука не стоит на месте. И в наше время, во многих развитых странах ведутся исследования и разработки по созданию новых типов аккумуляторов, главная задача которых — повышение энергоёмкости.
 ТОП-theMEN. Мужской блог Блог для настоящих мужчин
ТОП-theMEN. Мужской блог Блог для настоящих мужчин




